治疗ND4突变引起的Leber遗传性视神经病变
-
NFS-01 (NR082, rAAV2-ND4)目前阶段:
中国完成3期临床患者入组,美国完成1/2期首例患者入组
下一个里程碑:中国3期临床数据,美国完成1/2期患者入组
-
NFS-02 (rAAV2-ND1)
治疗ND1突变引起的Leber遗传性视神经病变
目前阶段:完成中美1/2期临床试验首例患者入组
下一个里程碑:完成中美1/2期临床试验所有患者入组
(Leber hereditary optic neuropathy, LHON)
该疾病是一种母系遗传的线粒体疾病,多发于14-21岁的青年男性,患者表现为双目视力受损至失明。这一疾病由德国眼科医生 Theodor Leber于1871年首先发现,目前全球患者约60万人,其中中国10万人。LHON是线粒体DNA突变所导致的疾病,位于线粒体基因组上的第11778、第14484和第3460位点为该病的3个原发位点,90%以上的LHON病人中能够发现G11778A (ND4基因)、G3460A(ND1基因)、T14484C(ND6基因) 三个位点突变中的一个,尤以G11778A最多,占50%~80%。由于该突变使线粒体生物呼吸链受损,造成ATP缺乏,使患者视神经节细胞产生氧化应激,导致细胞凋亡。目前临床上尚无针对Leber遗传性视神经病变的有效疗法或治愈手段。
-

正常视野
-

一般病人视野
-

严重病情病人视野
纽福斯目前正在开发两款针对LHON的候选药物 - NFS-01(NR082, rAAV-ND4) 和 NFS-02(rAAV-ND1), 分别治疗G11778A (ND4) 位点突变和G3460A(ND1) 位点突变所引起的LHON疾病。作用机制为采用基因治疗策略,以重组腺相关病毒作为载体,将正确的基因通过玻璃体腔注射递送至患者受损的视神经节细胞,修复线粒体生物呼吸链,使视神经节细胞恢复活力与视功能。
纽福斯创始人李斌教授团队自2008年起即开始对眼科基因治疗技术的研究探索,于2011年发起全球首例LHON基因治疗研究者发起临床试验(IIT1), 并于2017年启动全球最大样本量基因治疗国际多中心研究者发起临床试验 (IIT2),至今已积累全球最长随访时间和最大样本量的安全性、有效性数据,为LHON候选药物的产业化开发提供有利支持。
LHON已于2018年5月被纳入国家《第一批罕见病名录》,纽福斯LHON候选药物的开发有望享受一系列罕见病药物研发鼓励政策;另外,NFS-01(NR082, rAAV-ND4)于2020年9月获得美国FDA孤儿药认定,为该产品加速国际化开发奠定了基础。
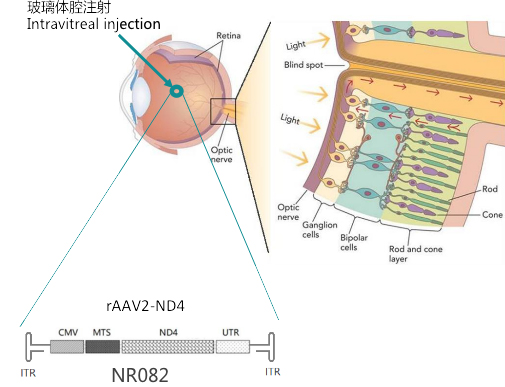
NFS-01 (NR082, rAAV-ND4)治疗LHON作用机理:
采用基因治疗策略,以重组腺相关病毒(rAAV)作为载体,将正确的ND4基因通过玻璃体腔注射递送至患者受损的视神经节细胞,修复线粒体生物呼吸链,使视神经节细胞恢复活力与视功能。
李斌教授团队通过两项研究者发起的临床试验(IIT1 & IIT2)证实NFS-01在人体内长期安全有效
| IIT1: SEE4LHON | IIT2: 4-HOPE | |
|---|---|---|
| 入组时间 | 2011-2012 | 2017-2018 |
|
ClinicalTrials.gov 登记号 |
NCT01267422 | NCT03153293 |
| 试验候选药物 | NR082 (rAAV2-ND4) | |
| 治疗剂量 |
0.5 x 1010 vg/eye for < 12 y.o. 1.0 x 1010 vg/eye for ≥ 12 y.o. |
1.0 x 1010 vg/eye for ≥ 6 y.o. |
| 受试者数目 | 9 | 159 |
| 受试者来源 | 9例中国 (亚洲) |
149例中国 (亚洲) 10例阿根廷 (非亚洲) |
|
单次注射后 随访时间 |
最长至90个月 | 最长至12个月 |
全球首个LHON临床试验和最长随访记录 IIT1:SEE4LHON
2011年,在纽福斯创始人、时任华中科技大学同济医学院眼科主任医师李斌教授的领衔下,全球首例针对Leber遗传性视神经病变的试验性NFS-01 (NR082, rAAV2-ND4)基因治疗临床试验(NCT01267422)在中国启动。科学家们以重组腺相关病毒作为载体,将正确的人ND4基因通过玻璃体腔注射递送至患者受损的视神经节细胞,修复线粒体生物呼吸链,使视神经节细胞恢复活力与视功能。
在参与试验的9例G11778A (ND4) 位点突变LHON患者中,5位患者的视力得到明显改善,最佳视力恢复到0.8,9名患者平均最佳矫正视力提高0.39logMAR (即接近字母表四行的提高)。其中8名患者完成了近8年的长期随访,无严重不良反应事件,且5名患者的视力改善一直被保持至今。该临床试验创全球眼科基因治疗最长随访记录,试验结果先后发表于2016年的《自然》子刊Scientific Reports 、2016年的《柳叶刀》子刊EBioMedicine 、及2020年的眼科领域顶级杂志《眼科学》上,并于2020年美国基因与细胞治疗学会(ASGCT)年会上报告 。
-
图为李斌教授在全球首个LHON临床试验
中为受试者注射NR082(rAAV2-ND4) -

图为IIT1研究结果在
EBioMedicine封面刊登
全球最大样本量基因治疗LHON临床试验 IIT2: 4-HOPE
在首项研究取得可喜成果后,李斌教授团队于2017-2018年间进行了一项更为全面的临床研究,研究入组受试者达159例(其中包括来自阿根廷的10例),这也是据公开资料显示迄今全球最大样本量的基因治疗临床试验。同样,十二个月随访结果显示候选药物疗效显着,且未发现严重不良反应。其中143名受试者完成一年随访,其中81名(56.6%)注射眼视力水平显著提高,该81名有效受试者平均视力提高达 0.57 LogMAR (视力表5-6行)。这项国际研究结果于2020年美国基因和细胞治疗学会(ASGCT)会议上进行了口头报告。
- Wan, X., Pei, H., Zhao, M. et al. Efficacy and Safety of rAAV2-ND4 Treatment for Leber Hereditary Optic Neuropathy. Sci Rep,2016; 6:21587
- Yang S., Ma S., Wan X., et al. Long-term outcomes of gene therapy for the treatment of Leber's hereditary optic neuropathy. EBioMedicine. 2016;10:258–268
- Yuan, J., Zhang, Y., Liu H., et al., Seven-year follow-up of gene therapy for Leber’s Hereditary Optic Neuropathy. Ophthalmology, 2020; 127(8):1125-1127
- 2020, ASGCT 23rd Annual Meeting. Oral presentation: First China International Gene Therapy Study in Leber’s Hereditary Optic Neuropathy (Abstract #1307)
- 2020, ASGCT 23rd Annual Meeting. Poster: Multiyear Follow-up of AAV2-ND4 Gene Therapy for Leber’s Hereditary Optic Neuropathy (Abstract #621)